| Практическая работа №7 Тема: Расчет материального и теплового балансов производства синтез -газа паро-кислородной конверсией метана | |
| Автор: drug | Категория: Прочее | Просмотров: | Комментирии: 0 | 11-08-2013 15:04 |
Практическая работа №7
Тема: Расчет материального и теплового балансов производства синтез -газа паро-кислородной конверсией метана
Цель: Составить и рассчитать материальный и тепловой балансы производства синтез-газа паро-кислородной конверсией метана.
Теоретические основы
В настоящее время для получения синтез-газа широко используют метод конверсии метана. Конверсию можно проводить в водяным паром, с диоксидом углерода и с кислородом (окислительная конверсия).
СН4 + Н2О « СО + 3Н2
СН4 + СО2 « 2СО + 2Н2
СН4 + 0,5О2 « СО + 2Н2
При конверсии метана с водяным паром образующийся оксид углерода претерпевает дальнейшую конверсию до СО2. Таким образом, процесс конверсии метана с водяным паром позволяет получать газ любого состава (вплоть до чистого водорода), что достигается изменением соотношения исходных газов и температуры.
Конверсию метана с водяным паром или с диоксидом углерода проводят в трубчатых печах. Окислительную конверсию метана проводят в реакторах шахтного типа, заполненных катализатором.
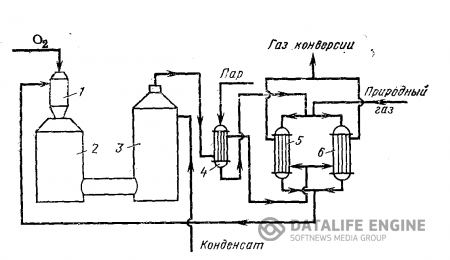
Рисунок 7.2 Технологическая схема получения синтез-газа парокислородной конверсией углеводородных газов
1 – смеситель; 2 – конвертор; 3- увлажнитель; 4 – пароперегреватель; 5,6 – теплообменники.
Природный газ, поступающий при давлении 0,4-0,5 МПа, дросселируют до 0,08-0,12 МПа и подают в теплообменники 5 и 6. На входе в теплообменники к газу примешивают водяной пар, перегреваемый с 180-3500С. После смешения парогазовая смесь имеет температуру 1800С. В теплообменниках ее нагревают до 3450С и затем направляют в вертикальный кожухотрубчатый смеситель 1, куда поступает также кислород. Из смесителя парогазовая смесь идет в конвертор 2 с никелевым катализатором ГИАП-3. Там при 800-9000С и 0,14 МПа протекают реакции конверсии с образованием синтез-газа. Конвертированный газ поступает в увлажнитель 3, куда впрыскивают водный конденсат (при этом температура газа снижается до 6500С). Затем газ проходит трубное пространство пароперегревателя 4, теплообменники 5 и 6 и, охладившись до 5000С, идет на конверсию оксида углерода (если требуется получать водород) или охлаждается до комнатной температуры и поступает в газгольдеры.
Задание
Составить материальный и тепловой балансы парокислородной конверсии природного газа.
Исходные данные:
Варианты заданий
|
Вариант |
СН4 , %(об) (х1) |
С2Н6, %(об) (х2) |
С3Н8, %(об) (х3) |
С4Н10, %(об) (х4) |
N2,%(об) (х5) |
|
1 |
98 |
0,4 |
0,03 |
0,15 |
1,42 |
|
2 |
97,8 |
0,5 |
0,2 |
0,1 |
1,4 |
|
3 |
97,5 |
0,6 |
0,25 |
0,2 |
1,45 |
- ·Степень конверсии углеводородов в пересчете на метан 95% (c).
- · На входе в конвертор отношение пар/газ равно 1,1 (V=110м3).
- · Состав технического кислорода 95% О2 (Х) и 5% (об.) N2 + Ar (Х).
- · Температура паро-газовой смеси на входе в конвертор 5500С(t1), на выходе 7500С(t2).
- · Температура кислорода 500С(tо2).
- · При определении состава конвертированного газа принять, что соотношение между СО и СО2 в нем соответствует равновесию реакции конверсии СО водяным паром.
- · Расчет проводим на 100м3 (V ) исходного сухого газа.
Порядок выполнения работы
Обозначим содержание (в м3) компонентов в конвертированном газе:
СО2 – ;
СО – в;
Н2 – с;
объем прореагировавшего водяного пара за вычетом образовавшегося за счет сгорания водорода – d;
х – расход технического кислорода.
Составим балансовые уравнения по содержанию каждого элемента в исходном и конвертированном газах.
- · Баланс по углероду, м3:
содержание углеводородов в исходном газе в пересчете на метан -
V= х1 + 2× х2 + 3× х3 + 4 × х4
содержание метана в конвертированном газе V = V × (1 - )
всего V = + в + V
отсюда + в = V- V (1)
- · Баланс, м3:
по водороду 2× х1 + 3 × х2 + 4 × х3 + 5 × х4 + V = с + V× 2 +(V - d)
отсюда находим (с – d) это будет уравнение (2)
по кислороду 0,5 × V + 0,95× х = + 0,5× в + 0,5× (V - d)
отсюда получим уравнение с неизвестными х, , в и d, это будет
уравнение (3)
Так как соотношение между СО и СО2 в конвертированном газе определяется равновесием реакции конверсии СО водяным паром при 7500С и 1×105 Па (1атм), когда К = 1,255. можно записать:
К= = = 1,255 (4)
Составим уравнение необходимое для определения неизвестных величин (уравнение теплового баланса конвертора):
∑Q = ∑Q
Приход теплоты
- · Теплота, проступающая с паро-газовой смесью при температуре t1, кДж:
Q1 = V× C× t1 + V× С× t1,
где V- количество природного газа (м3) , по которому ведется расчет (см. исходные данные);
C- средняя теплоемкость сухого газа при 5500С
(C= 2,15кДж/м3×град);
V- количество водяного пара в исходной газовой смеси, м3 (см. исходные данные);
С- средняя теплоемкость водяного пара при 5500С
(С= 1,598 кДж/м3×град);
t1 - температура паро-газовой смеси на входе в конвертор, 0С.
- · Теплота, вносимая техническим кислородом при температуре tо2, кДж:
Q2 = х × С× t,
где х - расход технического кислорода, м3(неизвестная величина);
С- средняя теплоемкость технического кислорода при 500С
(С= 1,296 кДж/м3×град);
t- температура кислорода, 0С (см. исходные данные).
- · Теплоту реакции Q3 определяем по закону Гесса.
Q3= ∆Н× + ∆Н× в + ∆Н× V + ∆Н× (V- d) - ∆Н× х1 - ∆Н× х2 -
- ∆Н× х3 - ∆Н× х4 - ∆Н× V,
где ∆Н- энтальпия СО2 (∆Н=17600кДж/м3);
- содержание СО2 в конвертированном газе, м3 (неизвестная величина);
∆Н- энтальпия СО (∆Н= 4930кДж/м3);
в - содержание СО в конвертированном газе, м3(неизвестная величина);
∆Н- энтальпия СН4 (∆Н= 3300кДж/м3);
V - содержание метана в конвертированном газе, м3;
∆Н- энтальпия водяного пара (∆Н= 10800кДж/м3);
V- количество водяного пара в исходной газовой смеси, м3 (см. исходные данные);
d - объем прореагировавшего водяного пара за вычетом образовавшегося за счет сгорания водорода, м3 (неизвестная величина);
х1 - количество СН4 в исходном газе, м3 (см. таблицу варианты заданий);
∆Н- энтальпия С2Н6 (∆Н= 3680кДж/м3);
х2 - количество С2Н6 в исходном газе, м3(см. таблицу варианты заданий);
∆Н- энтальпия С3Н8 (∆Н= 4520кДж/м3);
х3 - количество С3Н8 в исходном газе, м3(см. таблицу варианты заданий);
∆Н- энтальпия С4Н10 (∆Н= 5480кДж/м3);
х4 - количество С4Н10 в исходном газе, м3 (см. таблицу варианты заданий).
Примечание: количество х1, х2, х3, х4 в м3 равно количеству х1, х2, х3, х4 в %(об), так как расчет ведется на 100м3 исходного сухого газа.
Подставляя известные значения, получим значение Q3 в кДж с тремя неизвестными , в, d.
Q = Q1 + Q2 + Q3
Расход теплоты
- · Теплота, уносимая конвертированным газом, кДж:
Q4 = × С× t2 + в × С× t2 + с × С× t2 + С×V× t2 + (х5 + 0,05×х)× С× t2 +
+ (V - d)× C× t2,
где - содержание СО2 в конвертированном газе, м3 (неизвестная величина);
С- средняя теплоемкость СО2 при 7500С (С=2,107кДж/м3×град);
t2 - температура паро-газовой смеси на выходе из конвертора, 0С (см. исходные данные);
в - содержание СО в конвертированном газе, м3(неизвестная величина);
С- средняя теплоемкость СО при 7500С (С= 1,38 кДж/м3×град);
с – содержание водорода в конвертированном газе, м3 (неизвестная величина);
С- средняя теплоемкость водорода при 7500С (С= 1,317 кДж/м3×град);
С- средняя теплоемкость метана при 7500С (С= 2,42 кДж/м3×град);
V - содержание метана в конвертированном газе, м3;
х5 - количество азота в исходном газе, м3 (см. таблицу варианты заданий);
х - расход технического кислорода, м3(неизвестная величина);
С - средняя теплоемкость азота и аргона при 7500С
(С= 1,37 кДж/м3×град);
V- количество водяного пара в исходной газовой смеси, м3 (см. исходные данные);
d - объем прореагировавшего водяного пара за вычетом образовавшегося за счет сгорания водорода, м3 (неизвестная величина);
C- средняя теплоемкость водяного пара при 7500С
(C=1,65 кДж/м3×град).
Подставляя известные значения, получим значение Q4 в кДж с неизвестными , в, с, d, х.
- · Принимая теплопотери Q5 равными 4% от прихода (по практическим данным), составим уравнение теплового баланса конвертора
0.96 × Q = Q4
Подставляя известные значения Q и Q4 получим уравнение (5) с неизвестными х, , в, d, с.
Подставляем в уравнение (5) значения в, d, х из уравнений (1), (2) и (3), получаем уравнение (6) – значение , выраженное через неизвестное с.
Заменяя в уравнении (6) на , выраженное через в из уравнения (1), находим в, выраженное через неизвестное с – это будет уравнение (7).
Подставляя в уравнении (4) значения , в, d, выраженные через с из уравнений (6), (7) и (2), находим неизвестное значение с.
Затем находим неизвестные значения , в, d, х.
- · Определяем количество азота и аргона, поступающее с техническим кислородом, м3
V = x × 0,05
Определяем количество азота и аргона в конвертированном газе, м3
V= х5 + V ,
х5 - количество азота в исходном газе, м3 (см. таблицу варианты заданий).
Таблица 7.1 – Состав сухого конвертированного газа
|
Компоненты |
%(об) |
м3 |
кг |
|
СО2 СО Н2 СН4 N2 + Ar |
|
в с V V
|
G G G G G |
|
Итого |
100 |
∑V |
∑G |
Примечание: Количество компонентов сухого конвертированного газа в кг определяем по формулам:
G=; G= ; G=; G=; G=
- · Составляем материальный баланс конвертора
Таблица 7.2 – Материальный баланс конвертора
|
Наименование |
м3 |
кг |
|
1 |
2 |
3 |
|
Приход 1. Природный газ СН4 С2Н6 С3Н8 С4Н10 N2 2. Водяной пар 3. Кислород технический О2 N2+Ar |
х1 х2 х3 х4 х5 V
х - V V |
|
|
Итого |
|
|
|
1 |
2 |
3 |
|
Расход
1. Сухой газ СО2 СО Н2 СН4 N2+Ar
2. Водяной пар
|
в с V V V |
G G G G G G |
|
Итого |
|
|
Примечание: Количество компонентов природного газа, количество водяного пара и технического кислорода в кг определяем по формулам:
G= ; G= ; G= ; G=; G=;
G= ; G= ; G= .
Количество израсходованного водяного пара определяем по формуле:
G= (G+ G+ G+ G+ G+ G+ G+ G) - ∑G
V=.
- · Объемное отношение пар/газ в газе после конверсии метана составляет:
n =
Зная , в, с, d, х, находим значения статей теплового баланса, оставшиеся неизвестными, в кДж – Q2, Q3, Q4
- · Потери теплоты в окружающую среду:
Q5 = Q× 0,04
- · Составляем тепловой баланс конвертора
Таблица 7.3 – Тепловой баланс конвертора метана
|
Наименование |
кДж |
% |
|
Приход
1. Теплота паро-газовой смеси 2. Теплота технического кислорода 3. Теплота реакций
|
Q1 Q2 Q3 |
|
|
Итого |
|
100 |
|
Расход
1. Теплота влажного конвертированного газа 2. Теплопотери
|
Q4
Q5 |
|
|
Итого |
|
100 |
Контрольные вопросы:
1. Перечислите методы получения синтез-газа.
2. Какой метод получил наибольшее распространение?
3. Как можно проводить конверсию метана для получения синтез-газа?
4. В каких аппаратах проводят конверсию метана водяным паром или диоксидом углерода?
5. В каких аппаратах проводят окислительную конверсию метана?
- Практическая работа №6 Тема: Расчет материального и теплового балансов производства водорода и синтез-газа парокислородной газификацией нефтяных остатков
- Практическая работа №8 Тема: Расчет трубчатой печи для конверсии природного газа в производстве водорода.
- Практическая работа 5 Тема: Расчет материального баланса колонны синтеза аммиака.
- Практическая работа 3 Тема: Расчет материального баланса установки получения метилового спирта.
- Практическая работа №1 Тема: Расчет материального и теплового балансов производства серы